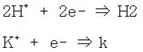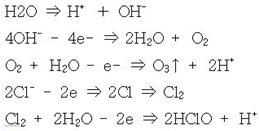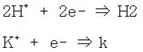산화전해수의 정의
가정용알칼리 전해수가 활성탄으로 염소를 제거한 물에 글리세린산 칼슘을 첨가하여 약한 전류를 통과시켜 전기분해한
음용, 피부세정 목적의 물인데 반하여, 강산성수는 물에 순도 99.0% 이상의 NaCl(식염) 또는 Kcl(염화칼륨)을 첨가하여
전기분해 했을 때 전극의 양극관 쪽에서 얻어지는 살균, 소독 목적의 물이다.
특성
| 구분 |
수도수(지하수) |
산화전해수(강산성수) |
환원전해수(강알칼리수) |
| pH |
6.8 ~ 7.7 |
2.4 ~ 2.7 |
11 ~ 12 |
| 차아염소산(ppM) |
0.3 |
10 ~ 20 |
0.4 |
| 산화환원전위(ORP) |
350 ~ 350mV |
1100 ± 20mV |
-700mV 이상 |
| 용존산소(ppM) |
9.2 |
25 |
- |
| O-NMR 반치폭 |
140 ~ 150Hz |
55 ~ 62Hz |
55 ~ 65Hz |
| 전도율(ms/cm) |
245 |
1,980 |
2,630 |
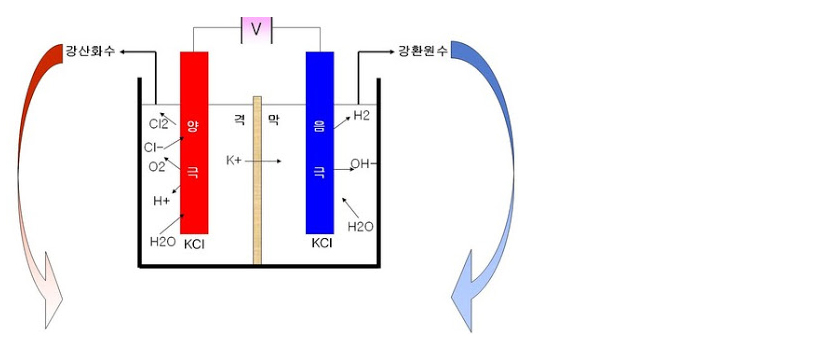
생성원리
- 전기적 성질을 가진 이온만 통과할 수 있는 특수이온 격막을 이용하여
- 양극실에서는
· 음(-)의 전기를 띤 이온(OH-,Cl-등)이 전자(e-)를 전극에 빼앗기는 반응이 일어난다.
· 염소가스(C12)와 차아염소산(HClO)이 발생한다.
· 일부의 O2는 +전극에 e-를 주고 물과 반응하여 O3(오존)를 생성한다.
· OH- 이온의 감소와 H+이온의 증가로 pH가 감소된다.
· 이를 화학반응식으로 표시하면,
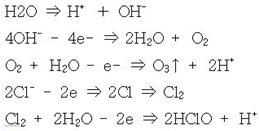
- 음극실에서는
· 양(+)의 전기를 띤 이온(CH+)이 전극으로부터 전자를 받아 수소가스가(H2)를 발생시키다.
· H+ 이온이 감소와 OH-의 이온의 증가로 pH가 상승한다.
· 전자(electron : e-)의 증가로 ORP는 떨어진다.
· 이를 화학반응식으로 표시하면,